Распределение Максвелла: как скорости молекул определяют физические свойства газов
Общая информация о распределении Максвелла
Распределение Максвелла широко используется для описания поведения газов в различных условиях. Оно позволяет определить, какие скорости наиболее вероятны для молекул газа при определенной температуре. Данные выводы играют важную роль во многих областях науки и техники, таких как астрофизика, аэродинамика, космическая техника, энергетика и другие.
Распределение Максвелла было открыто Джеймсом Клерком Максвеллом в 1860 году. В своей работе "На распределении скоростей молекул в газах" Максвелл показал, что для идеального газа, состоящего из множества молекул, распределение скоростей этих молекул может быть описано несколькими непрерывными функциями. Одной из них было именно распределение Максвелла. Позднее было выяснено, что аналогичные законы распределения существуют для других физических величин, таких как энергия и вероятность.
После открытия распределения Максвелла оно было широко применено в научных исследованиях, и в настоящее время остается одним из важнейших инструментов в различных областях науки и техники.
Распределения Максвелла
Распределение по вектору импульса
Формула распределения по вектору импульса:
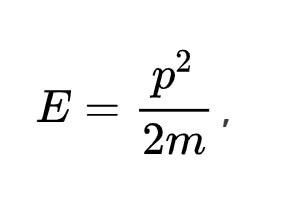
Распределение по абсолютной величине импульса
Формула распределения Максвелла-Больцмана по модулю скорости выражается через массу частицы, температуру и константу Больцмана:
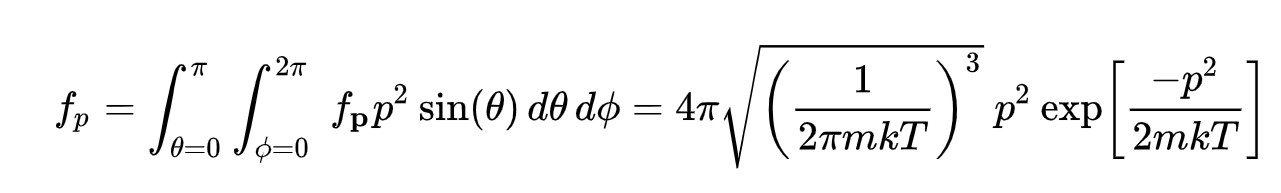
Распределение по энергии
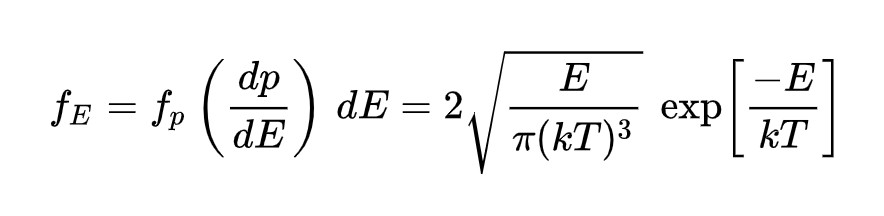
Распределение по модулю скоростей
Распределение по модулю скоростей описывает вероятность нахождения частицы системы с определенным значением абсолютной скорости. Оно является более интересным, чем распределение по проекциям скоростей, т.к. учитывает величину скорости независимо от ее направления. Для расчета вероятности используется функция плотности вероятности для модуля скорости. Поскольку модуль скорости всегда больше или равен нулю, то распределение его квадрата будет иметь хи-квадрат распределение с тремя степенями свободы.
Фрмула модуля скорости выглядит так:
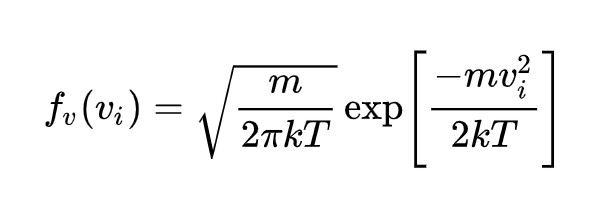
Эта формула описывает вероятность нахождения молекулы газа со скоростью v. Она показывает, что наибольшая вероятность нахождения молекулы газа приходится на значение скорости, равное корню квадратному из отношения 2kT / m. Это значит, что скорость молекулы газа зависит от температуры и массы молекулы, и чем выше температура газа, тем больше скорости молекул.
Применение распределения Максвелла
Кинетическая теория газов
Распределение Максвелла широко применяется в кинетической теории газов. Эта теория позволяет определять физические свойства газов, такие как давление, объем, температура, на основе движения и взаимодействия молекул в газе. Распределение Максвелла показывает, какие скорости молекул в газе наиболее вероятны, что позволяет оценить их средние значения и изменения при изменении условий.
Применение в научных и промышленных исследованиях
Распределение Максвелла используется в научных и промышленных исследованиях в различных областях, например, в космической технике оно используется для описания движения газовых частиц в космических аппаратах и ракетах, в астрономии - для изучения свойств звезд и галактик, а в химии - для анализа кинетических параметров химических реакций.Распределение Максвелла и статистическая физика
Связь с термодинамикой
Распределение Максвелла имеет тесную связь с термодинамикой. Согласно термодинамическим законам, температура системы является мерой средней кинетической энергии молекул в этой системе. Распределение Максвелла показывает, как распределены скорости молекул в системе при определенной температуре, что можно использовать для определения средней кинетической энергии.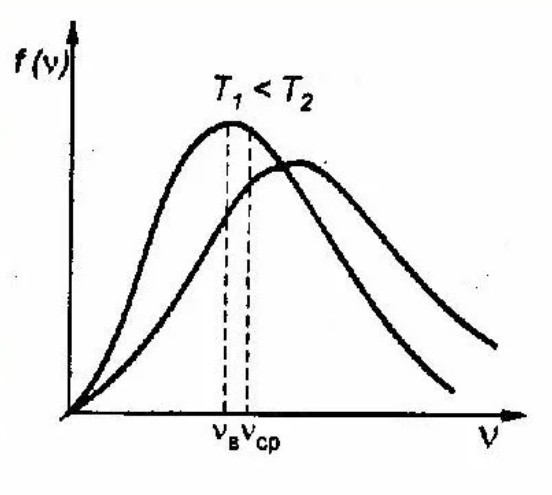
Статистическое описание распределения Максвелла
Особенности распределения Максвелла
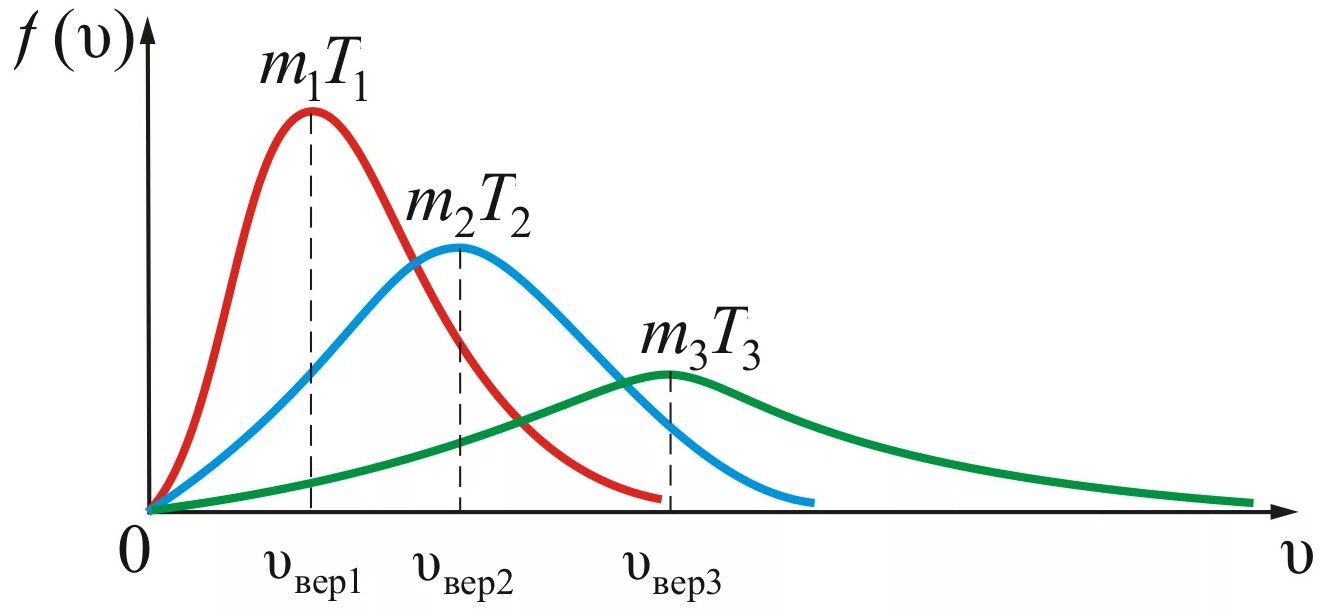
Параметры распределения
Как уже упоминалось, параметры распределения Максвелла зависят от массы молекулы и температуры газа. Чем выше масса молекулы, тем более узкое распределение скоростей, а чем выше температура, тем больше скоростей молекул, тем шире распределение скоростей.Графическое представление распределения Максвелла